主な研究活動の紹介
耳鼻咽喉科・頭頚部外科

研究代表者
耳鼻咽喉科・頭頸部外科特任部長
金丸 眞一

研究代表者
金井 理絵
- 研究テーマ
- 鼓膜再生の元になる組織幹細胞/前駆細胞の同定
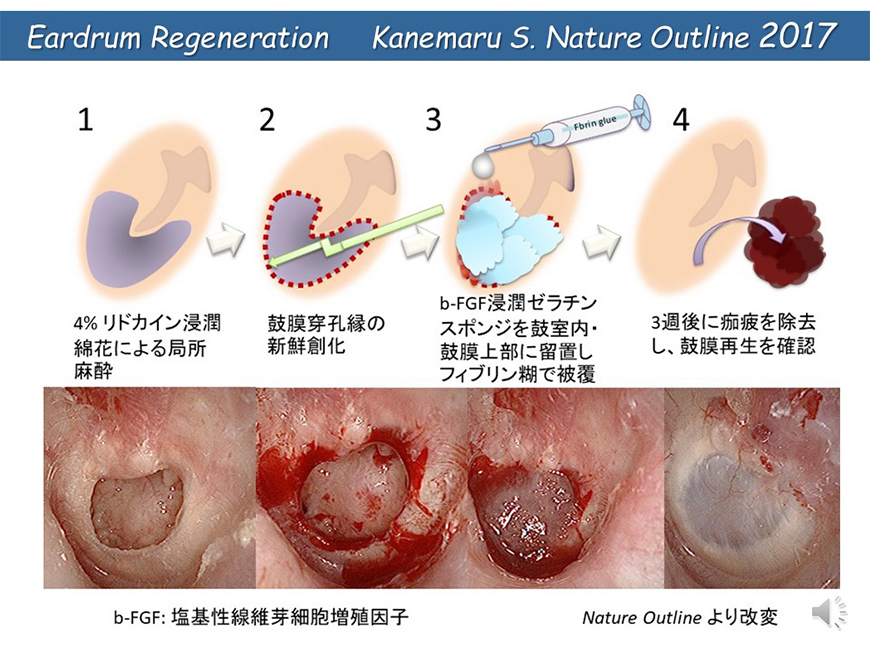
鼓膜再生を応用した新鼓室形成術の開発と外耳道軟部組織再生療法の開発
- 研究テーマ
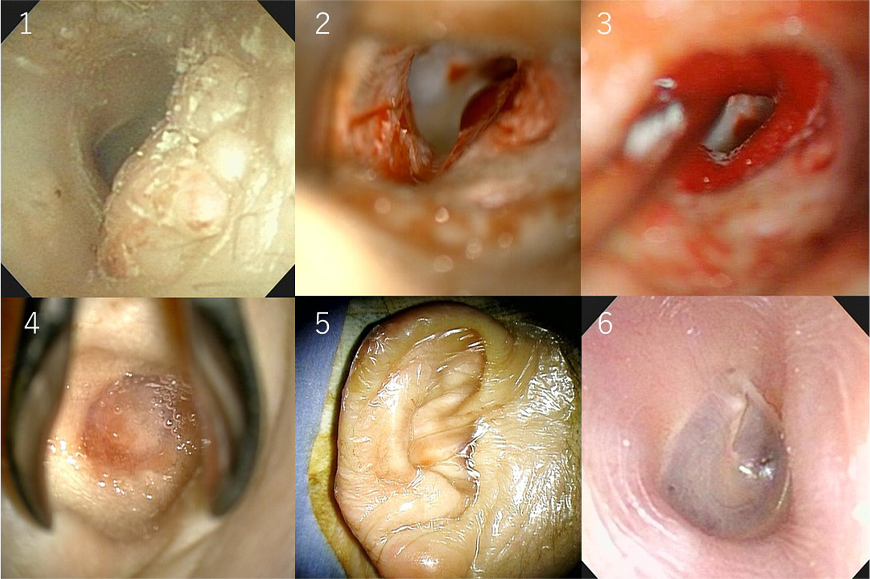
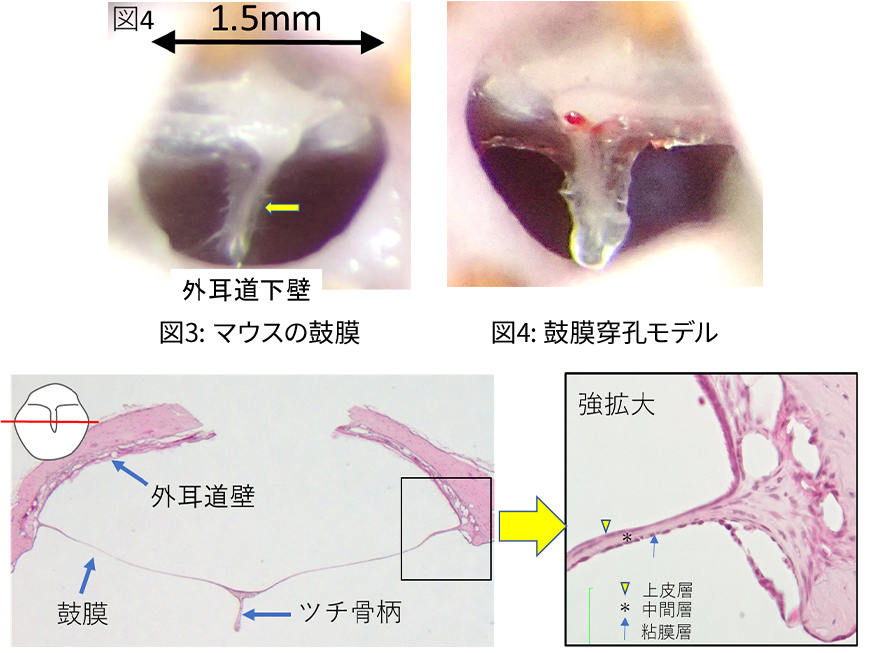
- マウス鼓膜穿孔閉鎖過程の細胞動態の解明
マウス鼓膜穿孔閉鎖過程の経時的変化
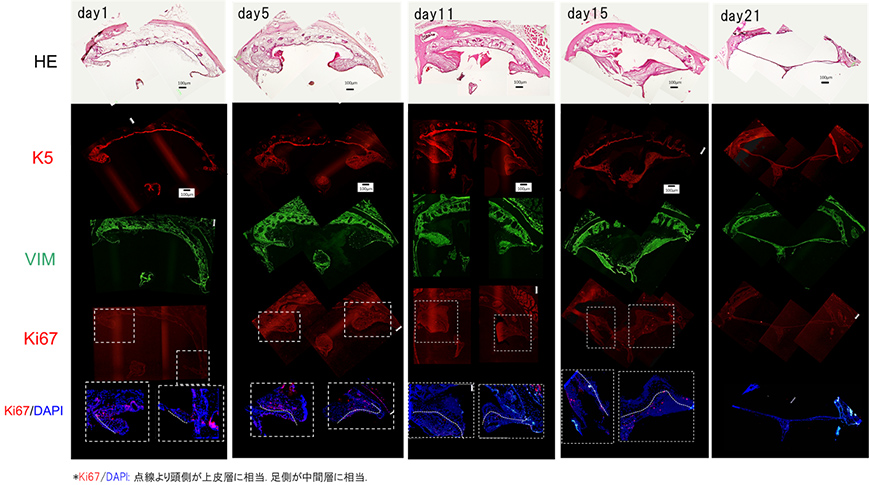
K5:Keratin5(上皮層のマーカー), VIM: Vimentin(中間層のマーカー), Ki67 (増殖能のマーカー)
歯科口腔外科

研究代表者
歯科口腔外科主任部長
高橋 克
- 研究目標
USAG-1に対する分子標的薬であるヒト抗USAG-1抗体を投与し、歯を萌出させる治療法を目指す。
- 研究テーマ
- 希少疾患先天性無歯症に対する歯数制御による歯の再生治療薬の開発。
PLoS ONE 11, e0161067. 2016
Inflammation and Regeneration, 40, 21, 2020
Sci Adv, 7, eabf1798, 2021
形成外科

研究代表者
形成外科部長
鈴木 義久
- 研究テーマ
- 末梢神経損傷を対象とする神経再生補助材の開発
- 研究目標
前立腺がん摘出後の海綿体神経叢損傷による勃起障害、子宮がん・直腸がん摘出後の骨盤神経叢損傷による排尿障害は生活の質の低下につながる。しかし、これら神経叢の損傷部の神経再生は不可能とされ放置されている。本研究の目的は、複雑な神経ネットワークを形成している神経叢の欠損の再建にも用いることのできるシート状の人工神経を開発することである。現在、共有結合架橋アルギン酸を用いてラットで有効性を評価している。
- 研究内容
ラットで、勃起障害・排尿障害が共有結合架橋アルギン酸を用いることで回復する結果が得られた。現在、PMDAの指導に基づき、非臨床POCデータを整え治験用プロトコール作成中である
- 研究テーマ
- 骨髄由来単核球を用いた脊髄損傷の治療
- 研究目標
中枢神経の再生は困難で、脊髄損傷の治療法は存在しない。骨髄由来細胞を用いた脊髄損傷治療法の有効性を証明することが目的である。
- 研究内容
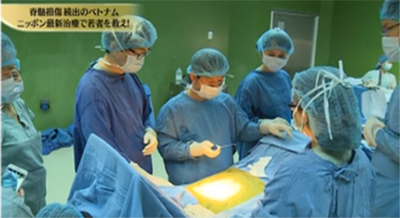
われわれは世界で初めて骨髄由来細胞を髄液内へ移植する方法を開発し臨床試験を行ってきた。現在、当院、滋賀医科大学、ベトナムダナン病院で臨床試験を行っている。ベトナムはバイク事故・転落事故が多く脊髄損傷が多発する。まず、ベトナムでの標準治療化を目指している。
呼吸器外科

研究代表者
黄 政龍
- 研究目標
基礎的研究やトランスレーショナル研究でえられた成果を、肺がん患者さんにおける臨床診療の現場に役立てることを目指しています。
- 研究テーマ
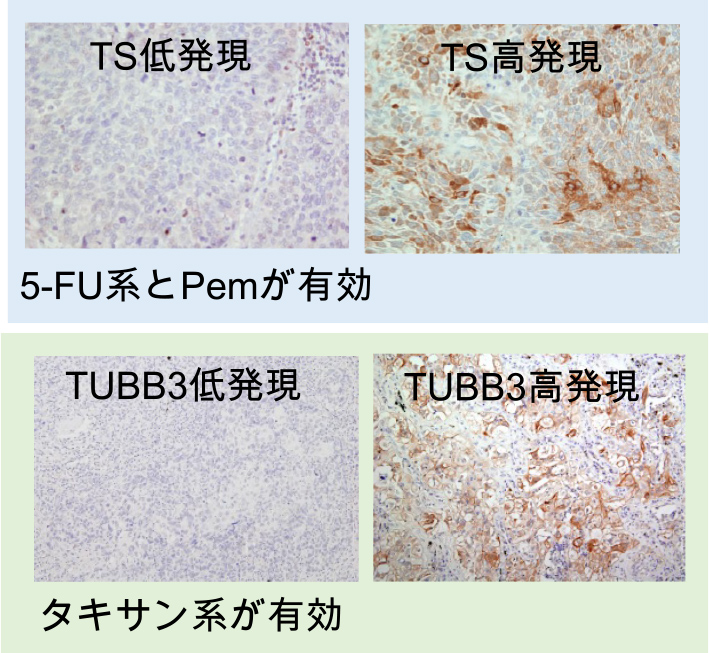
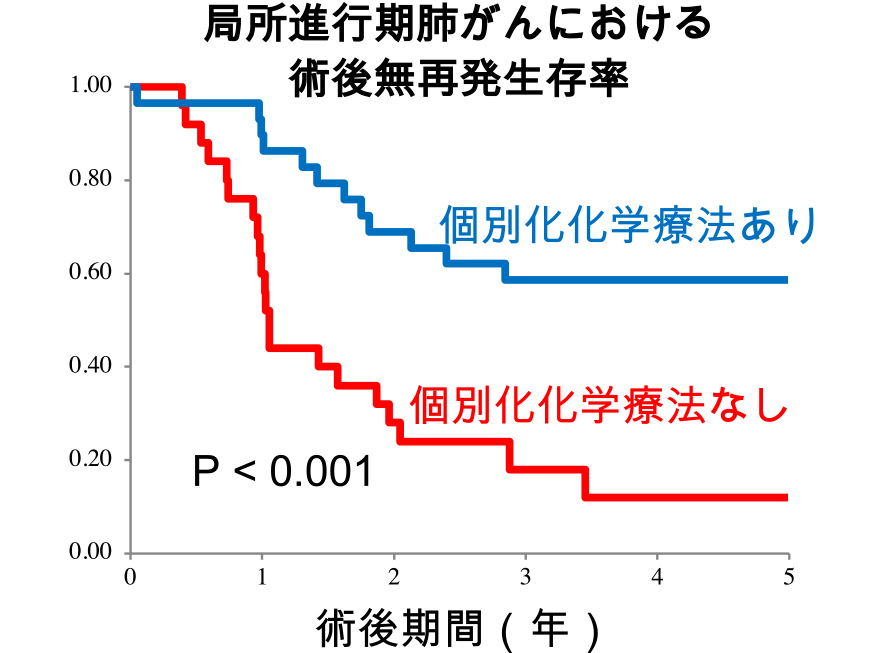
- バイオマーカーに基づく個別化化学療法
- 研究テーマ
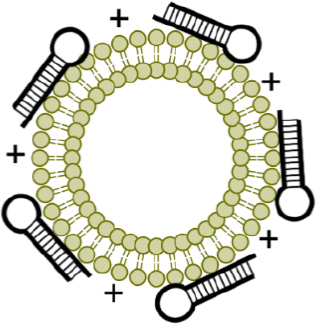
- バイオマーカーを標的とした核酸医療の開発
糖尿病内分泌内科

研究代表者
糖尿病内分泌内科部長・内分泌・代謝・腎臓研究部部長
濱崎 暁洋

研究代表者
糖尿病内分泌内科副部長・ 北野カデット研究員
渋江 公尊
研究者
本庶 祥子
綾野 志保
瀬野 陽平
長谷部 雅士
高橋 尚子
酒井 麻里子
研究目標
私たちは、代謝内分泌疾患診療の中で生じた疑問点から出発し、詳細な生理学的検査や分子レベルの解析を通じて、病態解明や個別化医療の推進に貢献する知見を得ることを目指します。
- 研究テーマ1
- 重症低血糖における膵α細胞機能及びグルカゴン作用に関する研究
- 研究内容
糖尿病の治療において重症低血糖は生命予後に関わる緊急性の高い病態であり、適切な治療と予防は我々の日常診療における最優先事項の一つです。低血糖からの回復には中枢神経を介した交感神経系の賦活化によるカテコラミンの増加や膵α細胞からのグルカゴン分泌などが関わっていることが知られています。糖尿病患者において低血糖からの回復機序がどのように変化しているかについては、1型糖尿病における自律神経障害(低血糖関連自律神経不全(HAAF))などの病態が研究されていますが、詳細なメカニズムについてはまだ解明されていない点が多く残されています。
私たちは低血糖回復機序を明らかにするため膵α細胞におけるグルカゴンに着目し、糖尿病においてグルカゴン分泌のメカニズム及びその作用がどのように障害されているかを臨床検体とin vitroモデルを組み合わせて明らかにすることを試みています。
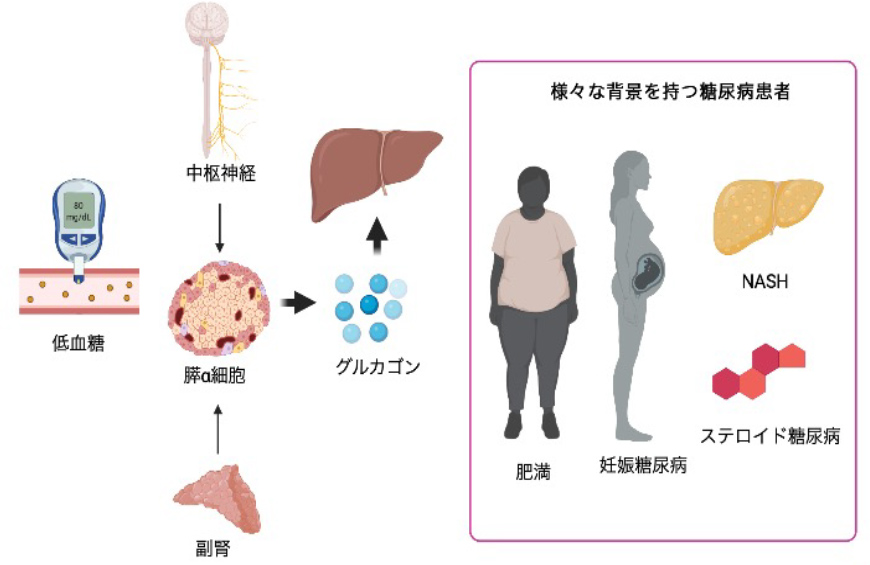
当科ではこれまでに食事グルカゴンを含むさまざまな臨床データにあわせた保存検体を有しており、また種々の負荷試験や詳しい病態生理解析を行う環境を整えています。 私たちはこれらのツールを組み合わせることで様々な背景を持つ糖尿病患者におけるグルカゴンの動態を明らかにすることを試みています。さらには特定の併存疾患・病態(肥満、NASH、ステロイド糖尿病、妊娠糖尿病、副腎疾患など)を持つ糖尿病患者におけるグルカゴンの作用がどのように変化しているかをグルカゴンの主な標的臓器である肝臓の細胞モデルを用いて分子生物学的側面から明らかにしていきます。
これらの研究を通して多様な疾患背景を持つ糖尿病患者様に対し、個々の病態に合わせた安全な低血糖の予防と治療法を提供することが私たちの研究の最終的な使命であると考えています。
- 研究テーマ2
- 代謝内分泌代謝疾患の新規バイオマーカー探索
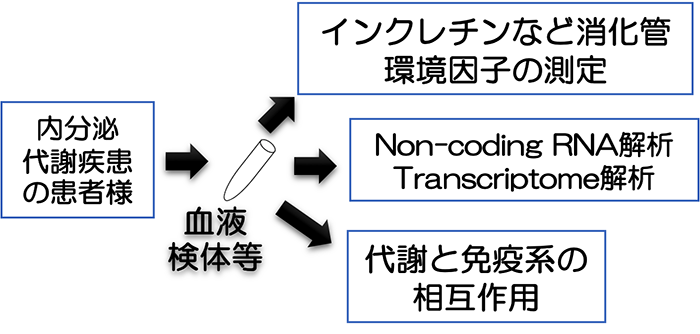
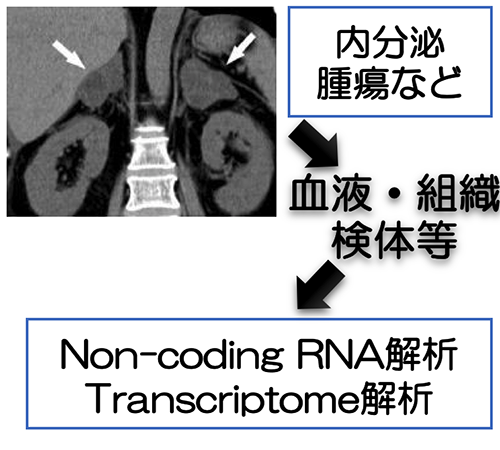
- 研究内容
代謝内分泌疾患の患者様の血液検体や手術検体を用いて、インクレチンなど消化管環境因子の測定や、transcriptome解析などを行っております。糖尿病の個別化医療や、機能性内分泌腫瘍の診断を推進する新規バイオマーカーを探索しています。
- 研究テーマ3
- 代謝内分泌疾患の遺伝子解析
- 研究内容
遺伝性代謝内分泌疾患の遺伝子診断体制の整備を進めています。
- 対象疾患
遺伝性カルシウム代謝異常、遺伝性内分泌腫瘍など

研究代表者
糖尿病内分泌内科副部長
泉 諒太
研究目標
インクレチンの多面的な作用の解明を通じて、よりよい糖尿病治療の確立を目指します。
- インクレチンについて
インクレチンは腸管から分泌されるホルモンで、GIP (glucose-dependent insulinotropic polypeptide)とGLP-1 (glucagon-like peptide-1)という2種類のホルモンが知られており、いずれもインスリン分泌を促進する物質として報告されています。このインクレチンに関連した薬剤が主に糖尿病薬、抗肥満薬として実際に使用されていますが、それだけではない多面的な作用を持つとされています。糖尿病治療においては、単に血糖を下げるのみならず、合併症の総合的な管理が必要となりますので、好ましい多面的作用の存在は、糖尿病治療にふさわしい薬剤としての新たな位置づけの根拠となります。
- 研究内容
 主にラットを用いた実験によりインクレチン関連薬の投与で生じる変化の解析を行っています。それに加えて、実際にインクレチン関連役を投与されている患者さんのデータと照合することで、動物実験で得られた知見がヒトへと応用可能であるか検討します。また、その効果をより引き出す薬剤を探索することにより、さらなる総合的な糖尿病治療法の確立を目指します。
主にラットを用いた実験によりインクレチン関連薬の投与で生じる変化の解析を行っています。それに加えて、実際にインクレチン関連役を投与されている患者さんのデータと照合することで、動物実験で得られた知見がヒトへと応用可能であるか検討します。また、その効果をより引き出す薬剤を探索することにより、さらなる総合的な糖尿病治療法の確立を目指します。
腎臓内科

研究代表者
腎臓内科副部長
半田 貴也
目的/展望
臨床現場で患者に接し続ける医師だからこそ可能な、研究と臨床の橋つなぎとなる研究を施行し、慢性腎臓病患者さんの治療に役立つ情報を提供する活動を目的とします
- 腎生検データベースを用いた病理学的解析と予後検討
当科では2000例を超す腎生検データベース・バイオバンクを抱える。我々は慢性糸球体腎炎患者の中で最多であるIgA nephropathyと比較し、高齢化に伴い増加が見込まれる類似疾患 IgA dominant IRGNが糸球体内の炎症細胞が多く、IgAが係蹄壁に沈着するという病理評価と腎予後・生命予後が悪いことを明らかにした。同意を頂いた患者様の医療情報とバイオバンクから、背景・病理学的解析や予後を評価し、新たなバイオマーカーの評価を施行しています。
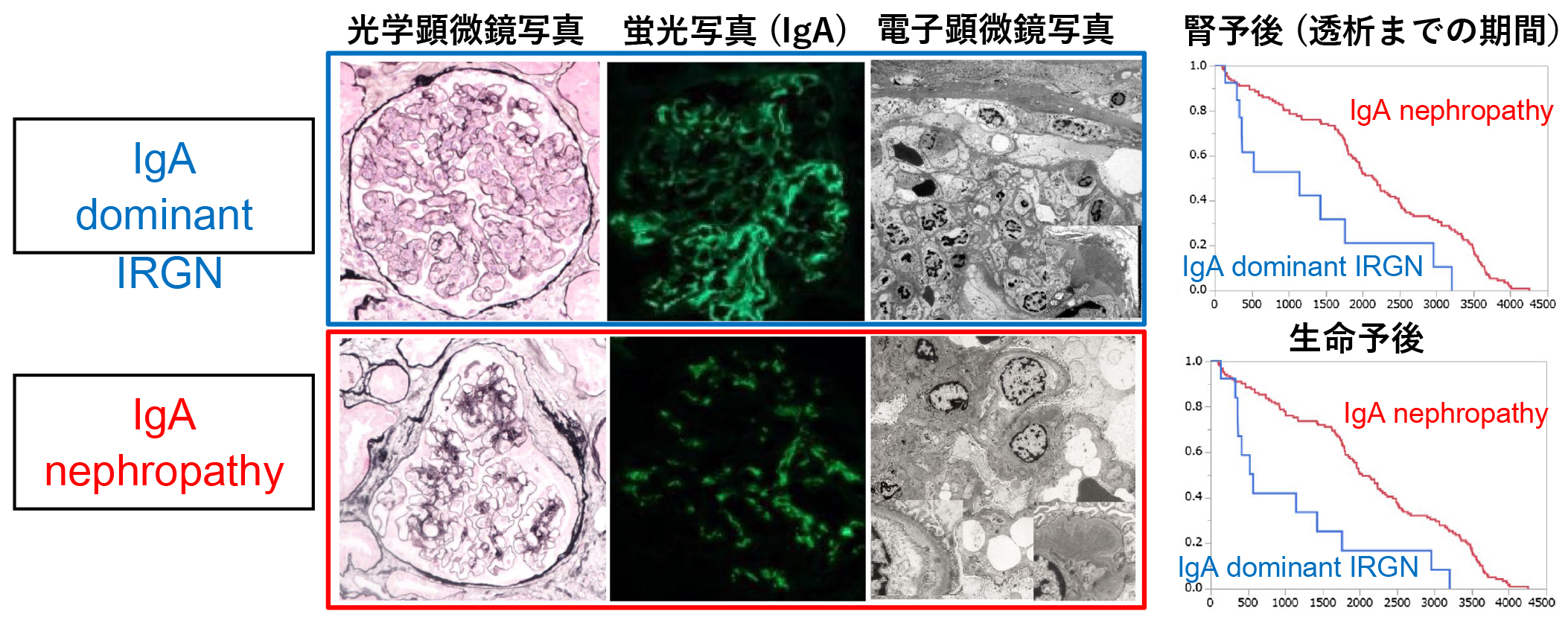
Takaya Handa et al. Clin Exp Nephrol. 2018 Oct;22(5):1116-1127
- 新規アフェレシス加療のサイトカインの評価
包括的高度慢性下肢虚血 は時に下肢切断に至る慢性虚血疾患であるが、新規アフェレシス加療としてレオカーナ®が知られる。我々はレオカーナ®の治療効果と血中サイトカイン(ブラジキニン)濃度の上昇が血圧変化と相関することを示した。今後もアフェレシス加療の液性因子と予後の評価を施行していきます。
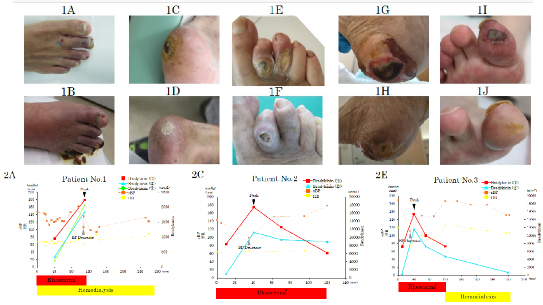
Takaya Handa et al.Ther Apher Dial. 2024 Jan 3.
消化器内科

研究代表者
消化器内科
森田 敏広
- 研究目標
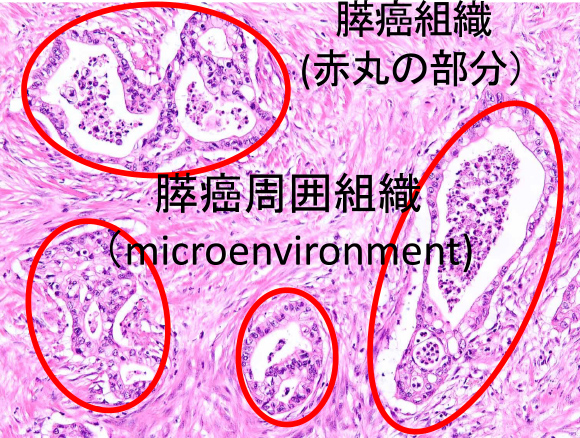
膵癌における新規バイオマーカーを発見する 膵癌および周囲組織(microenvironment)が形成されるメカニズム明らかにする
- 研究テーマ1
- 早期膵癌における新規バイオマーカーの探求および膵癌・周囲組織(microenvironment)形成のメカニズムの解析
- 背景
膵癌は未だに5年生存率が10%以下であり極めて難治性の疾患で、予後の改善には早期発見が不可欠です。膵癌は周囲に強い繊維化・新生血管などを伴うことを特徴としており(microenvironment)、繊維化による膵臓の萎縮を捉えることで早期発見につながる可能性がります。
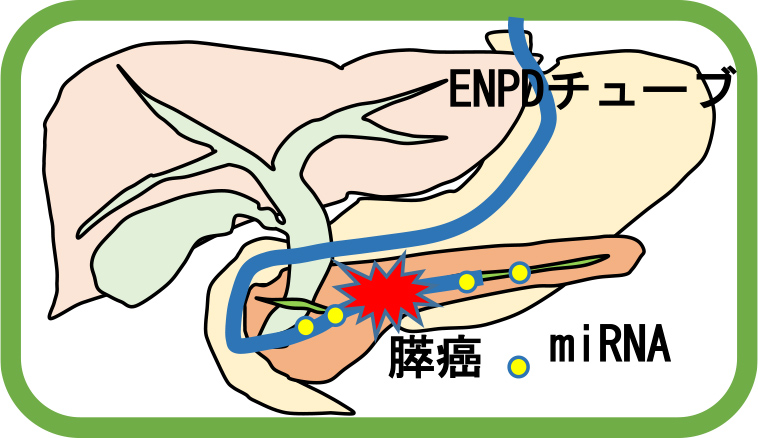
miRNAは遺伝子発現を調節するRNAの一種で、膵癌や周囲組織から分泌されることが知られてます。
膵癌・周囲組織から膵液に分泌されるmiRNAをとらえることで、早期膵癌の新規バイオマーカーになる可能性や、膵癌が形成されるメカニズムを解明できる可能性があります。
- 研究計画
膵管狭窄像や膵実質の萎縮・繊維化などにより早期膵癌が疑われた患者に対し、内視鏡検査を行い膵管ドレナージチューブ(ENPDチューブ)を留置しています。この際に膵液を回収させていただき、膵液中のmiRNAを測定し健常者と比較することで新規のバイオマーカーの候補となるmiRNAを探します。
また、候補となったmiRNAの機能を細胞株や実験動物などを用いて解析することで膵癌・周囲組織の形成におけるメカニズムを明らかにしていきます。
リウマチ膠原病内科

研究代表者
高橋 令子
- 研究目標
多因子が継時的に複雑に相互作用して病態を形成している自己免疫疾患、全身性エリテマトーデス(SLE)の病態の解明、「免疫学的寛解」の探索
- 研究テーマ1
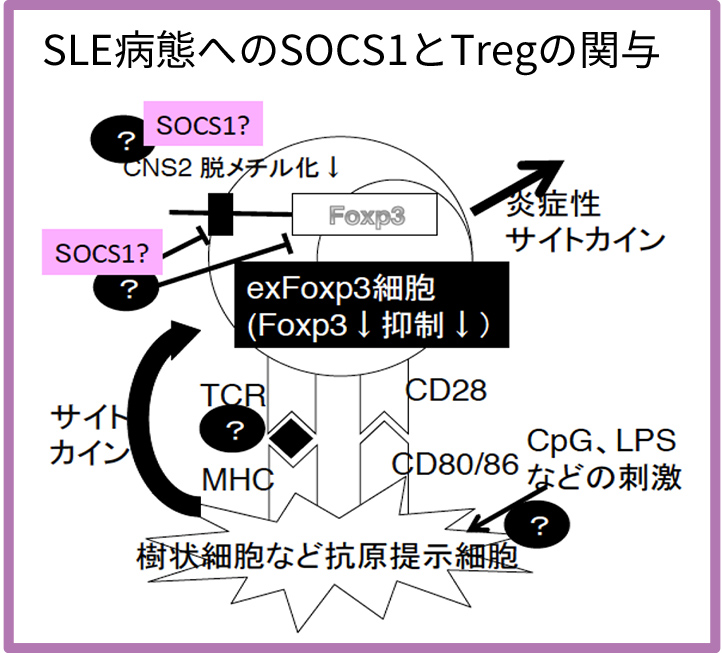
- SLE病態の安定維持に寄与するSOCS1 (Suppressor of cytokine signaling 1)などの因子の同定とその役割の解明
 背景
背景
代表者は、制御性T細胞(Treg)におけるSOCS1の可塑性防御による抑制機能維持の役割を解明してきた (Takahashi R JEM 2011, Takahashi R J. Immunol.2017)。これらの知見を元に、 SOCS1 のSLE病態への関与に関しての研究をさらに進め、SLE病態の再燃防止、安定維持の方法に発展させる。- 研究計画
- 患者血液、生検組織を用いて、 SLEの活動性とSOCS1発現動態の経時的変化、症状の重篤度とSOCS1発現量の相関、SLE患者におけるSOCS1の発現調節メカニズムなどを解析する。
- SOCS1欠損あるいはSOCS1トランスジェニックマウスなどのマウスを用いて、 SLE病態安定化に寄与するSOCS1の発現動態を解析する。
- SOCS1に加えて、 SLEの免疫学的平衡状態を維持する分子を同定し、その役割を解析する。
- 参考文献
Takahashi R, Nakatsukasa H, Shiozawa S, Yoshimura A. SOCS1 Is a Key Molecule That Prevents Regulatory T Cell Plasticity under Inflammatory Conditions.
J Immunol. 2017;199:149-158.
Takahashi R, Nishimoto S, Muto G, Sekiya T, Tamiya T, Kimura A, Morita R, Asakawa M, Chinen T, Yoshimura A.
SOCS1 is essential for regulatory T cell functions by preventing loss of Foxp3 expression as well as IFNg and IL-17A production.
J Exp Med. 2011;208:2055-67.
- 研究テーマ2
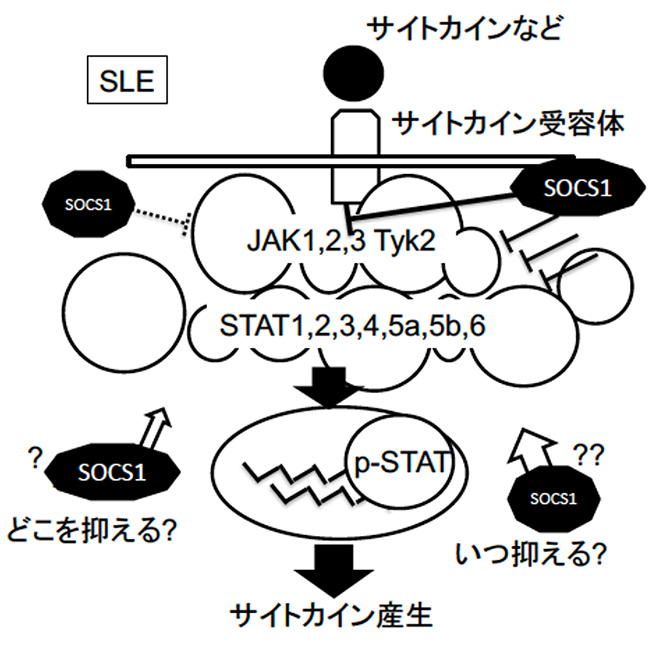
- SLEの免疫学的平衡状態の破綻、あるいは安定維持を司るサイトカイン関連分子の動態の解明
 背景
背景
SOCS1などの抑制性分子によるサイトカイン分子ネットワークの支配は複雑であり、どのように制御されているのか全貌は解明されていない (Yamada et al., Int Immunol (2006))。さらに、SLE患者病態でこれらサイトカインネットワークがどのように支配されているのか、どのようにこれらのネットワークを支配すればSLE病態を制御できるのか未解明である。サイトカイン関連分子の動態を解明することにより、 SLE病態の安定化維持に加えて、論理に基づいた至適免疫抑制施行による感染症や悪性腫瘍の発症の防御に発展させる。
- 研究計画
SLE患者末梢血などを用いたサイトカイン関連遺伝子と蛋白の発現定量解析を施行する。SLE患者の治癒過程で、これらの状態がどのように変化していくか、加えて病態との関連も解析し、統計学的解析にて重要分子、重要経路を探索する。
- 総括
免疫学的事象は、「正と負のバランス」が重要である。 SLE患者の病態制御で克服すべき問題の中で以下2点を重視する。1)不可逆的臓器病変の発症を防ぐためにも再燃させない治療方法の探索、2)非特異的治療に起因する感染症や悪性腫瘍の発症を防ぐ治療方法の探索である。目標達成のためには、このバランスの正確な理解が求められる。それらの知見を基に、SLEの「免疫学的寛解」とは何かを探索し、どのようにSLE病態を制御すべきかを解明する。
- 特徴
代表者は全国様々な施設にて、たくさんのSLE患者様の加療に携わって参りました。今後も、日々の診療で生じた気づきや疑問を基に、SLEの病因を解明すべく研究に邁進します。また、多くのSLE患者様が通院していらっしゃいます当院・研究所として、特に患者様の検体を用いた研究に注力して研究を進めます。将来、明解なSLEなど膠原病の原因を患者様とお話できることを切望しております。
消化器外科

研究代表者
消化器外科
井口 公太
- 研究テーマ
- 質量分析技術を応用した肝疾患バイオマーカー研究
- 研究目標
基礎研究・臨床研究にて抽出したバイオマーカーを、実際に患者さんの診療に役立てることを究極の目標としています。
- 研究内容①
肝臓癌や転移性肝癌の治療において中心的な役割を担っているのが肝切除です。肝切除は手技の向上等により安全に受けて頂けるようになりましたが、肝機能の悪い患者さん、あるいは大量に切除しなくてはいけない患者さんには肝不全を発症するリスクが存在します。ラット肝切除モデルにおいて、肝切除後肝再生をする動物と肝再生出来ずに肝不全死に至る動物では、何が臨界点・閾値となっているのか、肝臓内メタボローム(代謝物質)の観点から探っています。
- 研究内容②
食生活の欧米化に伴い、肝臓癌発症の原因としての、肥満・脂質代謝異常・高血圧等を主徴とするメタボリック症候群が注目されています。メタボリック症候群の肝臓における表現型である非アルコール性脂肪肝炎(NASH)を背景としたブタ発癌モデルを我々は作成しました。本ブタモデルを利用し、正常肝から脂肪肝、NASH、肝硬変、発癌に係る時間的過程を血液と肝臓内プロテオーム(タンパク質)を解析し、バイオマーカーの抽出を行っています。
- 特徴
ブタNASH肝癌モデルにて、血清二次元電気泳動の手法にて有意な変化を示すタンパク質としてITIH-4を抽出しました。ITIH-4は実臨床でも患者さんの予後に関連するマーカーとして妥当性が確認されました。
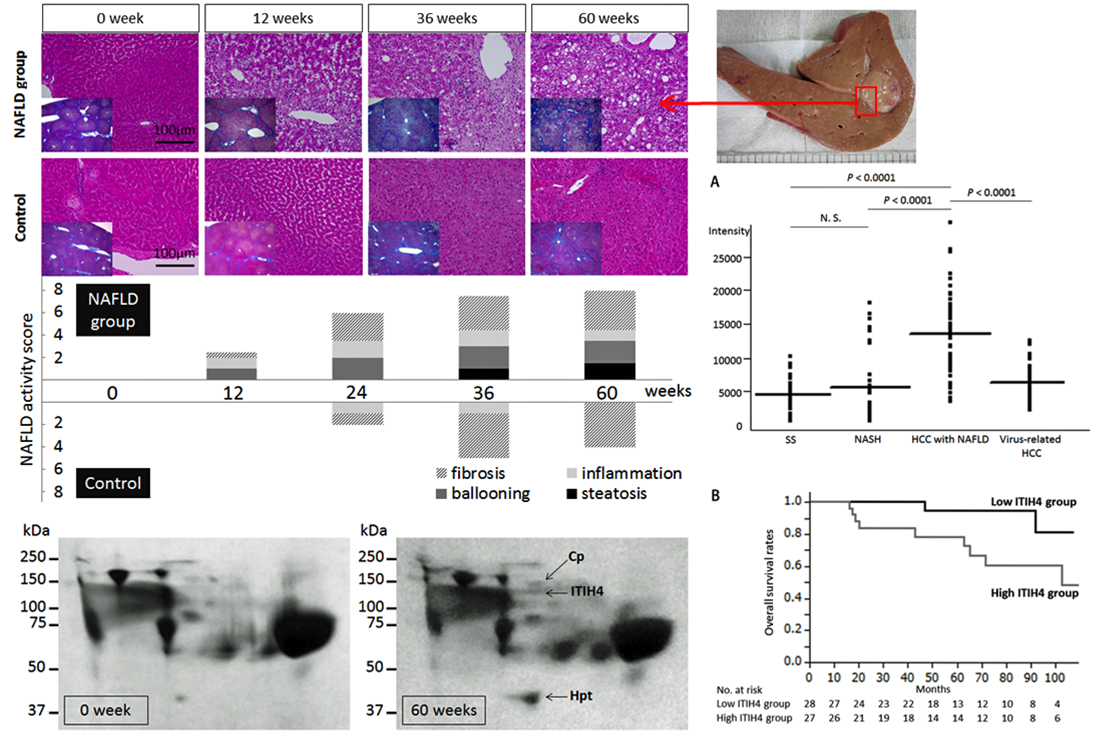
AASLD 2016発表 Manuscript in submission(Nakamura et al)

研究代表者
腫瘍研究部客員研究員
山本 健人
目標
大腸がんの患者さんに最新の未承認抗がん剤を使っていただけるように、がん細胞を培養して得られた遺伝学的データを用いた基礎研究を行っています。
- 大腸がんのがん細胞を培養する技術の応用
手術で摘出した大腸がん組織を利用し、「がん幹細胞スフェロイド」と呼ばれる特殊な形態でがん細胞を培養する技術を用いて研究います。 この方法を使うことで、「抗がん剤が効くか効かないか」を患者さんに投与する前に診断できたり、遺伝学的データを解析してどのようなタイプのがんかを正確に調べたりすることができます。 また、スフェロイドをマウスに移植し、抗がん剤を投与することで効果の判定を行うこともできるため、さまざまな応用が可能な手法です。
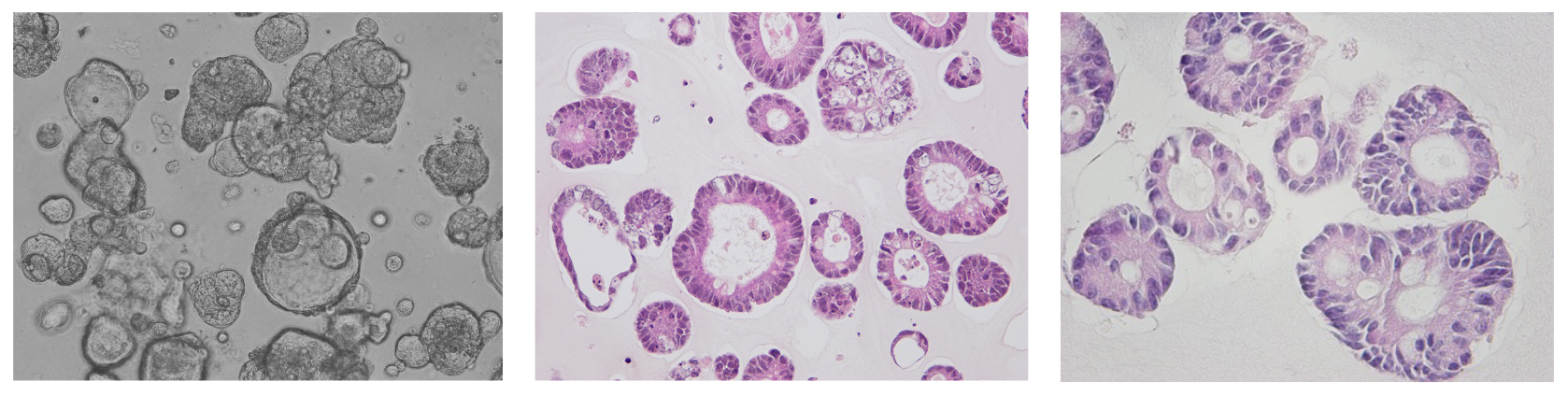
Yamaura T, Yamamoto T et al. Oncotarget. 2018, Miyoshi H et al. Oncotarget. 2018
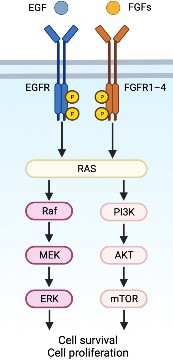
- 新しい抗がん剤「FGFR阻害薬」の臨床応用
がん細胞の表面にある「FGFR(線維芽細胞増殖因子受容体)」は、がん細胞の増殖に関わる重要なタンパクです。新規分子標的治療薬である「FGFR阻害薬」は、このタンパクをブロックすることでがん細胞の増殖を抑制できます。 現在、膀胱がんや胆道がんなどに使用されていますが、大腸がんには未承認です。 私たちは、どのような患者さんにFGFR阻害薬が効きやすいかを正確に診断する手法を開発し、大腸がん患者さんへのFGFR阻害薬の臨床応用を目指しています。
Kitano S, Yamamoto T, et al. Cancer Science 2022 Yamamoto T, et al. Cancers 2020

研究代表者
腫瘍研究部客員研究員、北野カデットメンター
京都大学 肝胆膵・移植外科 講師
内田 洋一朗
- 研究テーマ
- 虚血再灌流障害(Ischemia and Reperfusion Injury:IRI)の克服
IRIは血流低下と引き続く血液の再灌流により発症し、人間の全臓器において重要な課題である。
- 研究目標
我々のグループでは、肝臓外科領域(肝切除/肝移植など)における肝IRIを 克服すべく、そのメカニズムの解明、治療の開発、臨床への応用を目指しています。
- 研究体制
当研究グループ(消化器外科)は、2012年より、京都大学先端・国際医学講座(寺嶋宏明 客員教授/消化器外科主任部長)との連携大学院システムを構築。
京都大学肝胆膵・移植外科大学院生と共に研究を行っています(平尾浩史(UCLA留学)、門野賢太郎(UCLA留学)、宮内智之(客員研究員) 、川添 准矢(客員研究員)の4人の 医学博士を輩出。嵯峨謙一(大学院生)、田中康介(大学院生)、川本浩史(客員研究員)らを中心に研究中)。
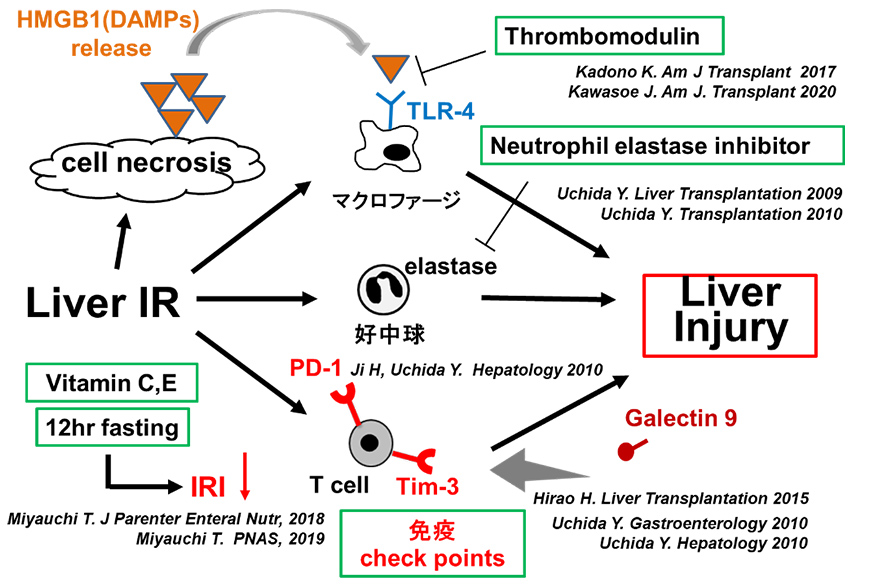
肝IRIに関与する細胞・分子について我々が報告してきたIRI抑制方法
- これまでの知見と展望
肝IRI克服(肝臓外科手術成績向上)には、極めてシンプルな短時間食事制限“fasting”が有効であることを発見しました(ケトン体(βヒドロキシ酪酸)が重要:2019 PNAS)。
食事制限による生体内変化(メタボローム解析)、消化管への作用(糞便細菌叢メタゲノム解析)、概日リズム(時計遺伝子)の解析などを行い、「食事制限による正の効果」の内因性分子機構を解明し、“外科周術期の最適な食事療法”と肝障害を軽減する薬物(分子)シーズの探索と確立を目指しています。
-

↑研究紹介クリック
外科医として熟練した高い外科技術を持ち、患者から信頼され、常に病気の解明と新規治療の開発研究にも情熱を傾ける外科医“Academic Surgeon”を目標とし臨床と研究に取り組んでいます。
Impact,2019
血液内科

研究代表者
腫瘍研究部客員研究員
京都大学血液内科
稲野 将二郎
- 研究目標
新しいがん治療のプラットフォームを作り出すことを目指しています。
- 研究テーマ1
- エクソソームを介した治療の開発
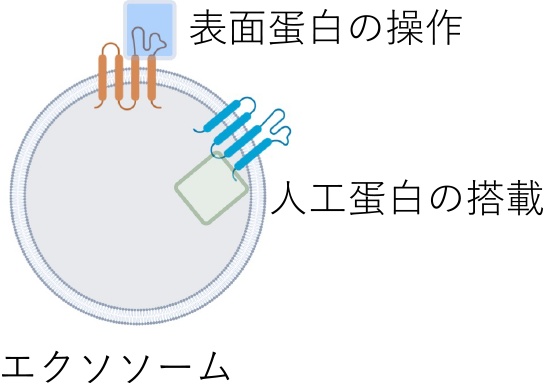 エクソソームは、細胞から分泌される直径100nm程度の小さな粒子ですが、細胞間のコミュニケーションに大きな役割を果たすことがわかっており、治療面でも注目が集まっています。エクソソームの表面蛋白を操作したり、治療用の蛋白を搭載することで、よりがん特異的な治療が可能になるよう、研究を行っています。
エクソソームは、細胞から分泌される直径100nm程度の小さな粒子ですが、細胞間のコミュニケーションに大きな役割を果たすことがわかっており、治療面でも注目が集まっています。エクソソームの表面蛋白を操作したり、治療用の蛋白を搭載することで、よりがん特異的な治療が可能になるよう、研究を行っています。
- 研究テーマ2
- がん原因蛋白を分解する人工蛋白の開発
- 現在、PROTACという、標的蛋白を分解する治療薬が多く開発途上にあります。革新的な薬ですが、残念ながら標的化が難しい対象が少なくありません。そこで、人工蛋白を使って、KRASやβカテニンなど、通常のアプローチでは困難ながん治療標的の分解を達成しました。この技術は異常蛋白が蓄積する神経変性疾患にも利用可能であり、がんに限らず臨床への還元を目指していきます。
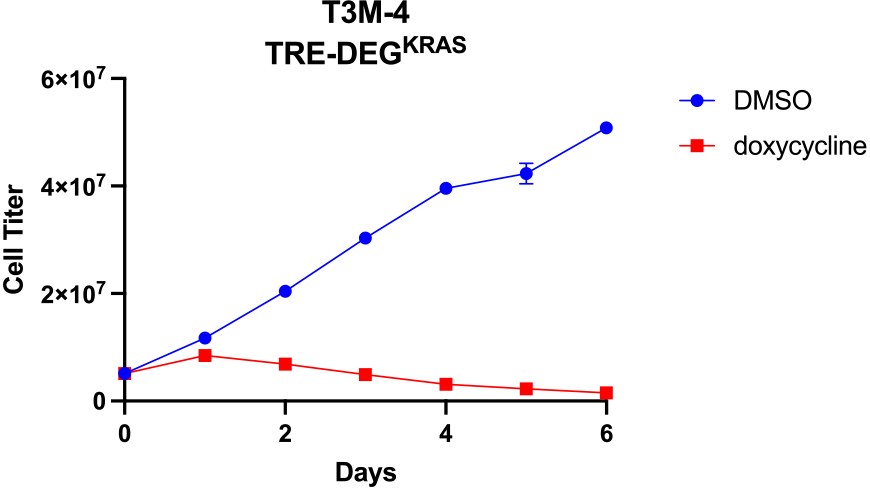
膵癌細胞株であるT3M-4に活性化型KRAS分解蛋白を発現させると、非常に強い増殖抑制が認められます。














 主にラットを用いた実験によりインクレチン関連薬の投与で生じる変化の解析を行っています。それに加えて、実際にインクレチン関連役を投与されている患者さんのデータと照合することで、動物実験で得られた知見がヒトへと応用可能であるか検討します。また、その効果をより引き出す薬剤を探索することにより、さらなる総合的な糖尿病治療法の確立を目指します。
主にラットを用いた実験によりインクレチン関連薬の投与で生じる変化の解析を行っています。それに加えて、実際にインクレチン関連役を投与されている患者さんのデータと照合することで、動物実験で得られた知見がヒトへと応用可能であるか検討します。また、その効果をより引き出す薬剤を探索することにより、さらなる総合的な糖尿病治療法の確立を目指します。






 背景
背景 背景
背景







