広くご活用いただくためにアクセス制限は設けておりませんが、内容は医学・医療関係者向けとなっており、一般の方のご利用は想定しておりません。
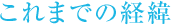
Cajalは「中枢神経である脳や脊髄は再生しない」としこの説は長い間広く信じられていました。1990年代、京都大学の川口先生等はラットを用いた脊髄の研究で「中枢神経も再生する」と発表しました。私たちも約15年前より、脊髄損傷の治療法の開発を開始しました。
- 人工材料(アルギン酸)を用いた脊髄再生の研究
海草より抽出した多糖類を特殊加工したマトリクスが脊髄再生に有効であることが分かった。【文献(1)(2)(3)(4)】
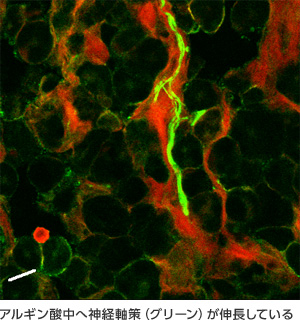
- 神経幹細胞を用いた脊髄再生の研究
神経の再生は認められたが移植した神経幹細胞の増殖が止まらず腫瘍化することが分かった。【文献(5)(6)】
脊髄内で神経系に分化する細胞の投与は4?5年後に腫瘍化する可能性があり(DOI:10.1371/journal.pmed.1000029)現時点では臨床使用できないと判断した。
- 細胞投与経路に関する研究
脳脊髄液中に投与した細胞は脊髄損傷部に到達し、再生に有効に作用していることが分かった。【文献(6)(7)】
細胞の静脈内投与も同様に簡便な方法である。しかし、大部分の細胞が肺にトラップされてしまう点、何年も経過した後肺の機能障害が有害事象として発生する可能性が高い点を解決する必要がある。また、全身の臓器へ細胞が供給されるため腫瘍化などの有害事象の追跡調査が困難である。
- 骨髄由来細胞(骨髄間質細胞、骨髄単核球)を用いた脊髄再生の研究
骨髄間質細胞、骨髄単核球を脳脊髄液中に投与することで機能回復が得られることが分かった。【文献(8)(9)(10)(11)(12)】
- 獣医科病院で実施されている骨髄由来細胞(骨髄間質細胞、骨髄単核球)を用いたイヌ損傷脊髄の治療
共同研究者である獣医師が有効性について論文発表した。【文献(13)(14)(15)】
- 急性期脊髄損傷に対する培養自家骨髄間質細胞移植による脊髄再生治療の検討(第I-II 相臨床試験)
5例に実施し終了した。【文献(16)(17)】
- 骨髄由来単核球細胞を用いた脊髄損傷に対する第I-II相試験
厚生労働大臣意見書(平成24年2月10日付け厚生労働省発医政0210第2号)に基づき実施を許可され、2012年3月より開始し2012年12月終了した。【文献(18)】
【対象となる患者さん】
- ・ 脊髄損傷の程度がASIA機能障害尺度(麻痺の程度で分類する基準)のA、B、C
- ・ 受傷後3週から1年までの部分的な脊髄損傷
- ・ 臨床試験での評価が可能な状態である
- ・ 同意取得時の年齢が20歳以上60歳以下
- 骨髄由来単核球細胞を用いた脊髄損傷(ASIA 機能障害尺度 A,B)に対する第II相試験
実施中
【対象となる患者さん】
- ・ 脊髄損傷の程度がASIA機能障害尺度(麻痺の程度で分類する基準)のA、B
- ・ 受傷直後から3ヶ月までの部分的な脊髄損傷
- ・ 臨床試験での評価が可能な状態である
- ・ 同意取得時の年齢が20歳以上60歳以下
- 平成25年11月11日
- 厚生労働省へヒト幹細胞臨床研究「骨髄由来単核球細胞を用いた脊髄損傷(ASIA 機能障害尺度 A,B)に対する第II相試験」を申請
- 平成26年8月6日
- 厚生労働大臣より意見書(「実施して差し支えない」)
- 平成27年1月1日
- 開始
問い合わせ希望の方は今かかっておられる主治医を通してご連絡ください

- 嗅球由来細胞の移植 (オーストラリアの病院等)
- ES細胞(Geron社:2010年10月開始、4人に実施され、2011年11月経済的理由で終了)
- 幹細胞(X-cell-Center: ドイツの幹細胞に対する法律が変わったため治療を終了)
- 大阪大学脳神経外科の嗅粘膜の移植:ポルトガルで開発実施されている方法
米国、エジプト、インドでも行われているようである。
- 脊髄損傷の再生治療についての記事が掲載されました。
- 産経新聞(2012年5月16日付 朝刊)
- 読売新聞(2012年5月16日付 朝刊)
- 毎日新聞(2012年5月17日付 朝刊)
- 中谷 壽男 〔京都大学医学部 S48年卒〕
- 関西医科大学 医学部 救急医学科診療科教授
- 井出 千束 〔東京大学医学部 S43年卒〕
- 藍野大学 医療保健学部 作業療法学科教授
京都大学名誉教授
- 福島 雅典 〔名古屋大学医学部 S48年卒〕
- (財)先端医療振興財団臨床研究情報センター センター長
京都大学名誉教授
- 大西 克則 〔京都大学医学部 S61年卒〕
- 医療法人西大路病院 神経内科医師
- Suzuki, K., Suzuki, Y., Ohnishi, K., Endo, K., Tanihara, M., Nishimura, Y. Regeneration of transected spinal cord in young adult rats using freeze-dried alginate gal. Neuroreport. 1999; 10, 2891-2894.
- Kataoka, K., Suzuki, Y., Kitada, M., Ohnishi, K., Suzuki, K., Tanihara, M., Ide, C., Endo, K., Nishimura, Y. Alginate, a bioresorbable material derived from brown seaweed, enhances elongation of amputated axons of spinal cord in infant rats. Journal of Biomedical Materials Research. 2001; 54, 373-384.
- Suzuki, Y., Kitaura, M., Wu, S., Kataoka, K., Suzuki, K., Endo, K., Nishimura, Y., Ide, C.: Electrophysiological and HRP-tracing studies of nerve regeneration through alginate-filled gap in adult rat spinal cord. Neuroscience Letters. 2002; 318, 121-124.
- Kataoka, K., Suzuki, Y., Kitada, M., Hashimoto, T., Chou, H., Bai, H., Ohta, M., Wu, S., Suzuki, K., Ide, C.: Alginate enhanced elongation of early regenerating axons in spinal cord of young rats. Tissue Engineering. 2004; 10, 493-504.
- Wu, S., Suzuki, Y., Kitada, M., Kataoka, K., Kitaura, M., Chou, H., Nishimura, Y., Ide, C.: New method for transplantation of neurosphere cells into injured spinal cord through cerebrospinal fluid in rat. Neuroscience Letters 2002; 318, 81-84.
- Wu, S., Suzuki, Y., Noda, T., Bai, H., Kitada, M., Kataoka, K., Nishimura, Y., Ide, C.: Immunohistochemical and electron microscopic study of invasion and differentiation in spinal cord lesion of neural stem cells grafted through cerebrospinal fluid in rat. Journal of Neuroscience Research 2002; 69, 940-945.
- Bai, H., Suzuki, Y., Noda, T., Wu, S., Kataoka, K., Kitada, M., Ohta, M., Chou, H., Ide, C.: Dissemination and proliferation of neural stem cells on the spinal cord by injection into the fourth ventricle of the rat: A method for cell transplantation. Journal of Neuroscience Method. 2003; 124, 181-187.
- Wu, S., Suzuki, Y., Ejiri, Y., Noda, T., Bai, H., Kitada, M., Kataoka, K., Ohta, M., Chou, H., Ide, C.: Bone marrow stromal cells enhance differentiation of cocultured neurosphere cells and promote regeneration of injured spinal cord. Journal of Neuroscience Research 2003; 72, 343-351.
- Ohta, M., Suzuki, Y., Noda, T., Ejiri, Y., Dezawa, M., Kataoka, K., Chou, H., Ishikawa, N., Matsumoto, N., Iwashita, Y., Mizuta, E., Kuno, S., Ide, C.: Bone marrow stromal cells infused into the cerebrospinal fluid promote functional recovery of the injured rat spinal cord with reduced cavity formation. Experimental Neurology. 2004; 187, 266-278.
- Yoshihara, T., Ohta, M., Itokazu, Y., Matsumoto, N., Dezawa, M., Suzuki, Y., Taguci, A., Watanabe, Y., Adachi, Y., Ikehara, S., Sugimoto, Y., Ide, C.: Neuroprotective effect of bone marrow-derived mononuclear cells promoting functional recovery from spinal cord injury. Journal of Neurotrauma. 2007; 24, 1026-1036.
- Nakano, N., Nakai, Y., Seo, TB., Yamada Y., Ohno, O., Yamanaka, A., Nagai, Y., Fukushima, M., Suzuki, Y., Nakatani, N., Ide, C.:Characterization of conditioned medium of cultured bone marrow stromal cells. Neuroscience Letters 2010; 483: 57-61.
- Ide, C., Nakai, Y., Nakano, N., Seo, TB., Yamada, Y., Endo, K., Noda, T., Saito, F., Suzuki, Y., Fukushima, M., Nakatani, T.:Bone Marrow Stromal Cell Transplantation for Treatment of Sub-acute Spinal Cord Injury in the Rat. Brain Res 2010; 1332: 32-47.
- Nishida, H., Nakayama, M., Tanaka, H., Kitamura, M., Hatoya, S., Sugiura, K., Suzuki, Y., Ide, C., Inaba, T.:Evaluation of transplantation of autologous bone marrow stromal cells into the cerebrospinal fluid for treatment of chronic spinal cord injury in dogs. Am J Vet Res 2011; 72: 1118-1123.
- Nishida, H., Nakayama, M., Tanaka, H., Kitamura, M., Hatoya, S., Sugiura, K., Harada, Y., Suzuki, Y., Ide, C., Inaba, T.:Safety of Autologous Bone Marrow Stromal Cell Transplantation in Dogs with Acute Spinal Cord Injury.Veterinary Surgery 2012; 41: 437-442.
- Tamura, K., Harada, Y., Nagashima, N., Kunimi, M., Itoi, T., Ishino, H., Yogo, T., Nezu, Y., Hara, Y., Suzuki, Y., Ide, C., Tagawa, M.:Autotransplanting of Bone Marrow-Derived Mononuclear Cells for Complete Cases of Canine Paraplegia and Loss of Pain Perception, Secondary to Intervertebral Disc Herniation. Experimental and Clinical Transplantation 2012; 3: 263-272.
- Saito, F., Nakatani, T., Iwase, M., Maeda, Y., Hirakawa, A., Murao, Y., Suzuki, Y., Onodera, R., Fukushima, M., Ide, C.:Spinal cord injury treatment with intrathecal autologous bone marrow stromal cell transplantation: The first clinical trial case report. The Jouranal of TRAUMA. 2008; 64, 53-59.
- Saito, F., Nakatani, T., Iwase, M., Maeda, Y., Murao, Y., Suzuki, Y., Fukushima, M., Ide, C.:Administration of cultured autologous bone marrow stromal cells into cerebrospinal fluid in spinal injury patient: a pilot study. Restrative Neurology and Neuroscience 2012; 30: 127-136.
- Suzuki, Y., Ishikawa, N., Omae, K., Hirai, T., Ohnishi, K., Nakano, N., Nishida, H., Nakatani, T., Fukushima, M., Ide, C.:Bone marrow-derived mononuclear cell transplantation in spinal cord injury patients by lumbar puncture. Restrative Neurology and Neuroscience. 2014; 32: 473-482.


